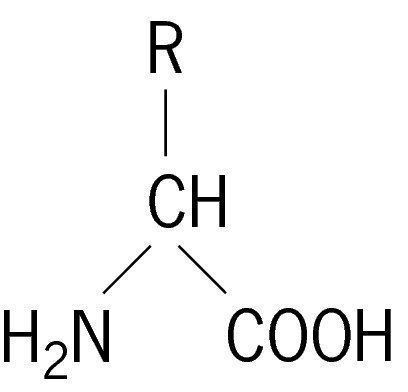
Den generelle formel for aminosyrer
Aminosyrer, hvis formuleringer overvejeskursus high school kemi, er vigtige stoffer til den menneskelige krop. Proteiner, der består af aminosyrerester, er nødvendige for at en person kan leve fuldt ud.

definition
Aminosyrer, hvis formler vil blive overvejetnedenfor er organiske forbindelser, hvori molekyler indeholder amino- og carboxylgrupper. Carboxyl består af en carbonyl- og hydroxyldel.
Du kan overveje aminosyrer som derivater af carboxylsyrer, hvor hydrogenatomet er erstattet af en aminogruppe.
Egenskaber af kemiske egenskaber
Aminosyrer, hvis generelle formel kan repræsenteres som CnH2nNH2COOH, er amfotere kemiske forbindelser.
Tilstedeværelsen af to funktionelle grupper i deres molekyler forklarer muligheden for manifestation af disse organiske stoffer af basiske og sure egenskaber.
Deres vandige opløsninger har egenskaberne af bufferløsninger. Zwitterion er et aminosyremolekyle, hvor aminogruppen er NH3 +, og carboxylen er repræsenteret som -COO-. Et molekyle af denne type har et essentielt dipolmoment, hvor den totale ladning er lig med nul. På sådanne molekyler er der opbygget krystaller af mange aminosyrer.
Blandt de væsentligste kemiske egenskaber i denne klasse af stoffer kan man udstikke polykondensationsprocesser, der resulterer i dannelsen af polyamider, herunder proteiner, peptider og nylon.
Aminosyrer, hvis generelle formel har formenCnH2nNH2COOH, reagere med syrer, baser, metaloxider, salte af svage syrer. Af særlig interesse er interaktionerne af aminosyrer med alkoholer relateret til esterificering.

Egenskaber af isomerisme
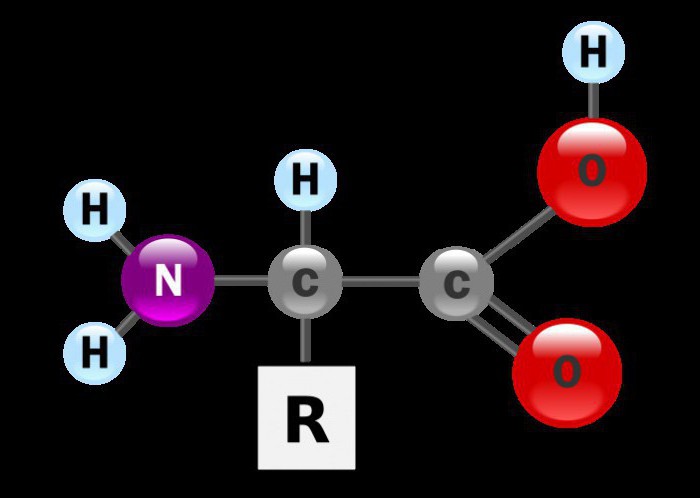
For at skrive de strukturelle formleraminosyrer bemærker vi, at mange aminosyrer, der deltager i biokemiske transformationer, indeholder en aminogruppe i a-stillingen fra carboxylgruppen. Et sådant carbonatom er et chiralt center, og aminosyrer betragtes som optiske isomerer.
Strukturen for aminosyrer giver en ide om placeringen af de vigtigste funktionelle grupper indeholdt i stoffet i forhold til det aktive carbonatom.
Naturlige aminosyrer, som er en del af proteinmolekyler, er repræsentanter for L-serien.
For optiske isomerer af aminosyrer er spontan langsom ikke-enzymatisk racemisering karakteristisk.

Egenskaber af a-forbindelser
Enhver formel af stoffer af denne type forudsætterposition af aminogruppen i det andet carbonatom. 20 aminosyrer, hvis formler anses for selv i skolens forløb af biologi, tilhører også denne art. For eksempel indbefatter de alanin, asparagin, serin, leucin, tyrosin, phenylalanin, valin. Det er disse forbindelser, der udgør den menneskelige genetiske kode. Udover standardforbindelser? Også i proteinmolekyler findes ikke-standard aminosyrer, som er deres derivater.
Klassificering ved syntese
Hvordan kan du adskille de essentielle aminosyrer? Formlerne i denne klasse er opdelt på basis af fysiologi i semi-udskiftelige, der kan syntetiseres i menneskekroppen. Isolere og de sædvanlige forbindelser, syntetiseret i enhver levende organisme.

Division af radikale og funktionelle grupper
Aminosyreformlen adskiller sig i strukturradikal (lateral gruppe). Der er en opdeling i ikke-polære molekyler indeholdende en hydrofob ikke-polær gruppe, såvel som ladede polære grupper. Som en særskilt gruppe i biokemi anses aromatiske aminosyrer: histidin, tryptofan, tyrosin. Afhængig af de funktionelle grupper skelnes der adskillige grupper. Alifatiske forbindelser er repræsenteret ved:
- monoaminomonocarbonforbindelser, såsom glycin, valin, alanin, leucin;
- hydroxymonokaminokarbonovymi stoffer: threonin, serin;
- monoaminocarbon: glutaminsyre, asparaginsyre;
- svovlholdige forbindelser: methionin, cystein;
- diaminomonokarbonovymi stoffer: lysin, histidin, arginin;
- heterocyklisk: prolin, histidin, tryptophan /
Enhver formel af aminosyrer kan skrives i en generel form, kun radikale grupper vil være forskellige.

Kvalitativ definition
For at opdage ubetydeligantal aminosyrer udføres en ninhydrinreaktion. Ved opvarmning af aminosyrer med en for stor mængde ninhydrin opnås et lilyprodukt, hvis syren har en fri a-aminogruppe, og den beskyttede gruppe er karakteriseret ved produktionen af et gult produkt. Denne teknik har en høj følsomhed, den anvendes til kolorimetrisk detektion af aminosyrer. På basis heraf blev der udviklet en distributionskromatografimetode på papir, indført af Martin i 1944.
Den samme kemiske reaktion anvendes iautomatisk analysator af aminosyrer. Enheden, der er oprettet af Moore, Shpakman, Stein, er baseret på adskillelsen af aminosyreblandingen i kolonner, der er fyldt med ionbytterharpikser. Fra søjlen strømmer eluenten ind i blanderen, og her kommer ninhydrin.
Intensiteten af den resulterende farve bedømmes på det kvantitative indhold af aminosyrer. Indikationer retter fotoelektrocolorimeteret, optageren registrerer.
En sådan teknologi er i øjeblikketDet bruges i klinisk praksis til blodprøver, cerebrospinalvæske, urin. Det giver mulighed for at give et komplet billede af den kvalitative sammensætning af aminosyrer indeholdt i biologiske væsker for at bestemme i dem ikke-standardiserede nitrogenholdige stoffer.
Nomenklatur Egenskaber
Hvordan korrekt at navngive aminosyrer? Formler og navne på disse forbindelser er angivet i IUPAC's internationale nomenklatur. Positionen af aminogruppen tilsættes til den tilsvarende carboxylsyre, begyndende med nummereringen fra carbonhydridet, der står under carboxylgruppen.
For eksempel er 2-aminoethansyre. Ud over den internationale nomenklatur findes der trivielle navne, der anvendes i biokemi. Så, aminoeddikesyre er glycin, der anvendes i moderne medicin.
I nærværelse af to carboxylgrupper i molekylet tilføjes suffikset-dionisk suffiks til navnet. For eksempel er 2-aminobutandisyre.
For alle repræsentanter for denne klasse er karakteristiskstrukturel isomerisme som følge af ændringer i strukturen af carbonkæden såvel som placeringen af carboxyl- og aminogrupperne. Foruden glycin (den enkleste repræsentant for denne klasse af iltholdige organiske stoffer)? De andre forbindelser har spejl antipoder (optiske isomerer).
ansøgning
Aminosyrer er almindelige i naturen, deer grundlaget for opbygning af dyr og planteproteiner. Disse forbindelser anvendes i medicin i tilfælde af alvorlig udtømning af organismen, for eksempel efter komplicerede kirurgiske operationer. Glutaminsyre hjælper med at bekæmpe nervesygdomme, og histidin bruges til at behandle mavesår. Ved syntetisering af syntetiske fibre (caproinsyre, enanth) virker aminocaproic og aminoenantinsyre som et råmateriale.
konklusion
Aminosyrer er organiske forbindelser,som i deres sammensætning har to funktionelle grupper. Det er de elementer i strukturen, der forklarer dualiteten af deres kemiske egenskaber, såvel som specifikationerne for deres anvendelse. Ifølge resultaterne af videnskabelige forsøg var det muligt at fastslå, at biomassen af levende organismer, der lever på vores planet, udgør 1,8 · 1012-2,4 · 1012 tons tørstof. Aminosyrer er de indledende monomerer i biosyntesen af proteinmolekyler, uden hvilke eksistensen af mennesker og dyr er umulig.
Afhængig af de fysiologiske egenskaberder er en underopdeling af alle aminosyrer i uerstattelige stoffer, hvis syntese ikke udføres i menneskekroppen og pattedyrene. For at undgå forstyrrelser i metaboliske processer er det vigtigt at forbruge fødevarer, hvori der er disse aminosyrer.
Det er disse forbindelser, der er ejendommelige"Mursten", som bruges til at opbygge biopolymerer-proteiner. Afhængigt af hvilken slags aminosyrerester, i hvilken rækkefølge der skal indbygges i proteinets struktur, har det dannede protein visse fysiske og kemiske egenskaber og anvendelsesområder. På grund af kvalitative reaktioner på funktionelle grupper bestemmer biokemikere sammensætningen af proteinmolekyler og søger nye måder at syntetisere individuelle biopolymerer til rådighed for menneskekroppen.
</ p>



